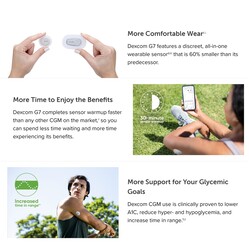
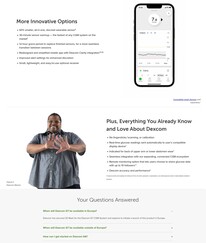
Milioni di utenti di monitor continuo del glucosio (CGM) stanno aspettando con ansia il sistema G7 di Dexcom. Il suo sistema CGM G6 ha dimostrato di essere molto popolare, offrendo un monitoraggio discreto del glucosio e la gestione tutto il giorno per gli utenti con diabete di tipo 1 o tipo 2, mentre anche facendo fuori i fastidiosi bastoncini per la maggior parte. Il Dexcom G7 promette numerosi miglioramenti rispetto al suo predecessore, tra cui essere il 60% più piccolo, offrendo un tempo di riscaldamento molto più veloce (30 min vs 120 min per il G6), e la combinazione del trasmettitore e del sensore.
Sembrava che la pandemia COVID-19 avesse rovinato il programma di rilascio del CGM usa e getta Dexcom G7, con la sua data di lancio effettiva che è praticamente un mistero. Tuttavia, è possibile che Dexcom si aspetta la palla per iniziare a rotolare molto presto, come una ricerca di Google per il G7 rivela una pagina bloccata https://www.dexcom.com/g7-ce-mark che era già stata creata per il monitor. Mentre la pagina attuale è vuota, la descrizione della ricerca di Google offre alcuni indizi
Dexcom G7 riceve il marchio CE - Introducendo il sistema CGM Dexcom G7...La prossima generazione Dexcom G7 può rendere la gestione del diabete potentemente semplice con un piccolo, all-in-one sensore indossabile e..
La pagina web bloccata è stata cached da Google, quindi può ancora essere visto, con screenshot forniti qui sotto per chi è curioso del G7 CGM. Il Dexcom G7 avrebbe dovuto ricevere il marchio CE richiesto per la produzione e la vendita nello Spazio economico europeo alla fine del 2021, cosa che può essere confermata dalla data di caricamento (21 dicembre) del video della dichiarazione "forward-looking" non quotata che è anche incorporata qui sotto. L'approvazione della FDA per il Dexcom G7 potrebbe arrivare nel 2022, anche se, come il CEO dell'azienda Kevin Sayer ha sottolineato in una recente intervista su https://www.medtechdive.com/news/dexcom-ceo-g7-launch-pandemic-pressure-international-markets/617246/la FDA sta sorprendentemente dando la priorità ai progetti legati a COVID-19 al momento.
Il G7 dovrebbe essere un sensore monouso di 10 giorni con potenziale per l'estensione a 14 giorni, e trasmetterà misurazioni continue del livello di glucosio a dispositivi intelligenti collegati nelle vicinanze. Il recente studio clinico ha mostrato che le letture della glicemia del Dexcom G7 erano +/- 20% di un risultato confermato prodotto utilizzando il metodo del bastoncino per il 93% del tempo, preso da 300 partecipanti che hanno accumulato 39.000 letture. Il costo è sconosciuto, ma il Dexcom G6 costa circa 3.800 dollari all'anno, quindi il G7 potrebbe essere simile. La buona notizia è che Medicare ha ampliato la sua copertura assicurativa per quanto riguarda i dispositivi CGM
I nostri Top 10
» Top 10 Portatili Multimedia
» Top 10 Portatili Gaming
» Top 10 Portatili Gaming Leggeri
» Top 10 Portatili da Ufficio e Business economici
» Top 10 Portatili Premium da Ufficio/Business
» Top 10 Portatili sotto i 300 Euro
» Top 10 Portatili sotto i 500 Euro
» Top 10 dei Portatili Workstation
» Top 10 Subnotebooks
» Top 10 Ultrabooks
» Top 10 Convertibili
» Top 10 Tablets
» Top 10 Tablets Windows
» Top 10 Smartphones
Fonte(i)
Google (Dexcom/pagina cached) & Non è solo una toppa & Dexcom & Fierce Biotech & MedTechDive